ISPE 是整个制药生命周期中科学、技术和监管进步的全球行业领导者。因此,ISPE 处于有利地位,可以协助美国政府、其盟友和志同道合的监管合作伙伴实施报告中提出的建议,建立有弹性的供应链,振兴美国制造业,以及培养广泛的基础成长:100 天评论。这些审查是由美国政府委托在四个具有重要战略意义的领域审查“美国的供应链”,其中之一是药物和活性药物成分 (API)。
COVID-19 大流行以及由此产生的经济混乱以及其他极端天气事件揭示了美国供应链中长期存在的脆弱性。由此产生的报告深入探讨了这些漏洞的原因,并得出结论,存在一组导致供应链漏洞的相互关联的主题和调查结果。这些是:
- 美国制造能力不足
- 私人市场中的错位激励和短期主义
- 盟国、伙伴国和竞争国采用的产业政策
- 全球采购的地域集中度
- 有限的国际协调
应美国联邦机构的要求,ISPE 与其愿景和使命保持一致,为复杂的制药行业挑战提供解决方案,并加强努力开发、制造和可靠地向患者提供优质药物,产生了相关的背景于2020 年 12 月发布的报告,提高基本活性药物成分供应的国内弹性。该报告由 14 位主题专家编写,可作为从事 100 天审查工作的药物和 API 工作组的资源报告。
100 天审查报告强调了以下两个与制药和 API 供应链可靠性相关的改进优先目标:
- 提高供应链透明度并激励弹性
- 提高美国和盟国药物制造和分销的经济可持续性。
ISPE 有一系列倡议和工作组,其中包含知识渊博的主题专家,他们正在制作材料,例如最佳实践指导文件、信息网络研讨会、演示文稿和与 100-日评论报告。这些团队的摘要如下图所示。

药物短缺
几乎 100 天审查报告的全部重点都与确定药物短缺的根本原因和减轻已确定风险的挑战有关。
自 2013 年以来,ISPE 的团队一直致力于该主题。已发表一系列报告和文章,以帮助行业分析药物短缺的潜在原因,并引入计划和程序以降低供应连续性的风险。一些关键的例子是:
- 2014 年 ISPE 药物短缺预防计划 – 一项可操作的计划,旨在帮助制药和生物制药行业避免因制造和质量问题导致的药物短缺。
- ISPE 药物短缺评估和预防工具,2015 年 – 为生物/制药行业的制造商提供了定位整个制药供应链当前和未来不一致的方法。通过使用该工具,制造商将在问题出现之前缓解问题,从而使他们能够为全球患者不间断地提供安全、优质的药物。针对以下六个维度中的每一个都引入了成熟度评估的概念:
- 企业文化
- 稳健的质量体系
- 指标
- 业务连续性规划
- 与当局的沟通
- 建设能力
- 防止药物短缺的业务连续性规划文章,2021 年 – 介绍了业务连续性规划的概念,即:
- 是一项多功能活动
- 对优先产品应严格
- 应评估产品特定风险和业务/运营风险
- 应该在存储/冗余与敏捷性之间取得平衡
- 不是一次性活动
- 可能受益于卫生当局的互动和反馈
ISPE 的药物短缺团队目前正在完成一项基准研究,该研究于 2021 年 5 月启动,该研究将用于评估业务连续性规划方面的最佳实践和行业成就,以防止药物短缺。该团队将使用匿名基准研究结果来确定优先级并开展活动,以通过改进业务连续性计划进一步支持行业。
即将于 2021 年 9 月 30 日星期四举行的网络研讨会“预防药物短缺的机会——行业和监管机构的观点”与 100 天审查报告特别相关。除了美国 FDA 的代表外,来自法国和巴西的监管机构以及来自 WHO 的代表也将出席。本次网络研讨会将:
- 让观众更好地了解推进药物短缺预防的关键机会,特别是在业务连续性规划和卫生当局参与领域。
- 聆听并探索全球卫生监管机构对药品短缺预防的当前思考。
- 分享有关可用于改善药物短缺预防的关键资源的信息,并激励公司寻求改进。
- 与 100 天审查报告部分“探索由国家战略储备管理的 API 储备和其他关键材料的虚拟战略储备的创建/扩展,包括成品剂量”相关,ISPE 有一个区块链特别兴趣小组,该小组正在审查应用区块链技术来帮助理解创建虚拟库存的挑战。
ISPE 继续在药物短缺评估和预防工具中确定的所有六个方面开展工作。另一个很好的例子是 ISPE 的提高药品质量 (APQ) 计划,该计划将在下面的“质量成熟度”标题下进行讨论。
创造质量透明度
质量成熟度
100 天审查报告包含以下对质量管理和质量成熟度的参考:
“ ………….与合作伙伴和盟友合作是建立健全和成熟的质量管理,以确保一致和可靠的药物生产和质量表现。以目前的形式,制药市场不承认或奖励对成熟质量管理的投资。”
“HHS 和 FDA 提议创建一个带有评级系统的计划,旨在认可和奖励成熟质量体系的制造商……。”
自 2018 年以来,ISPE 一直致力于一项名为提高药品质量(APQ) 计划的质量成熟度计划,该计划基于 ICH Q10,制药质量体系。这是一个行业对行业的计划,可以帮助公司、场所或部门了解他们的质量成熟度水平并进行改进,并且可以帮助组织为 FDA 或其他监管机构提出的任何质量管理评级系统做好准备。
2018 年制定的目标、好处和原则保持不变,APQ 计划的总体目标是:
- 整合质量管理成熟度、文化和卓越运营原则、工具和方法。
- 在合规之外培养质量的行业所有权。
- 促进资源的有效和高效利用。
- 支持和激励持续改进。
- 鼓励自我改进和供应商改进。
- 在公司之间实现结构化的基准测试、知识共享和学习。
- 提高优质产品供应的可靠性。
- 提供实现可持续竞争优势的途径。
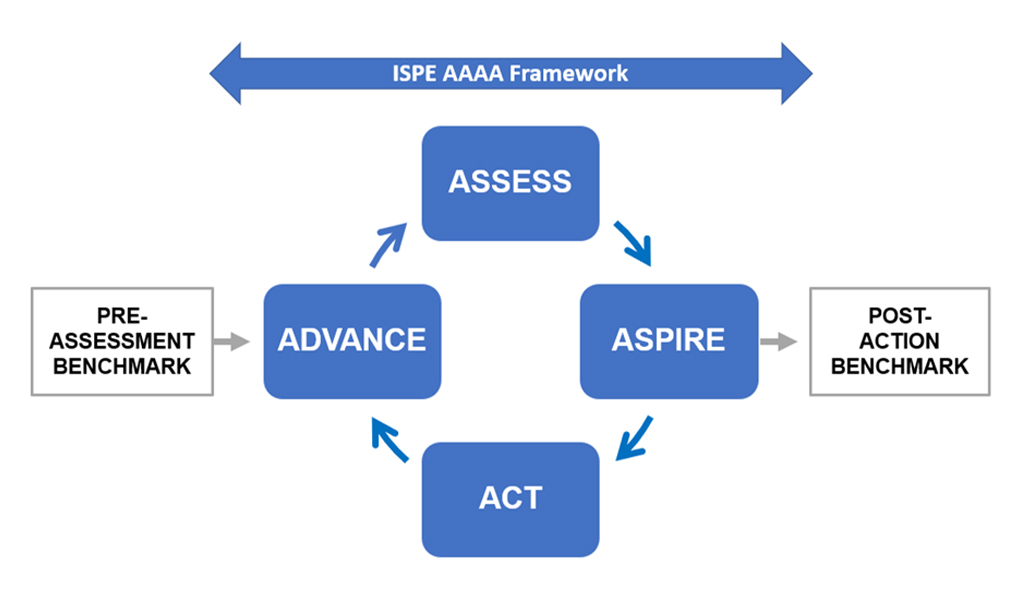
APQ 计划的设计以评估、渴望、行动和推进 (AAAA) 框架为核心,以提供正式的持续改进机会。评估允许建立基线并确定潜在的持续改进机会;渴望包括选择和优先考虑要采取的改进措施;行动需要制定详细的、资源丰富的行动计划,并有针对性地改进结果;而推进是评估并确认已实现所需的结果。
下图给出了包含 AAAA 框架的 APQ 计划。

APQ AAAA 框架是:
- 自我评估流程和工具包
- 由四个不同但相互关联的阶段组成
- 基于五步成熟度模型
- 旨在作为迭代的持续改进过程
- 详细的定量和定性案例研究,其中包含评估当前质量状态、诊断差距和确定改进机会的标准
为了提供定量基线,由圣加仑大学开发的 OPEX 基准测试工具被纳入 APQ AAAA 框架的基准测试前和基准测试后练习,如上图所示。该基准测试可以由 St. Gallen 选择执行,也可以使用 St. Gallen 在 APQ 指南中提供的工具自行应用来执行。
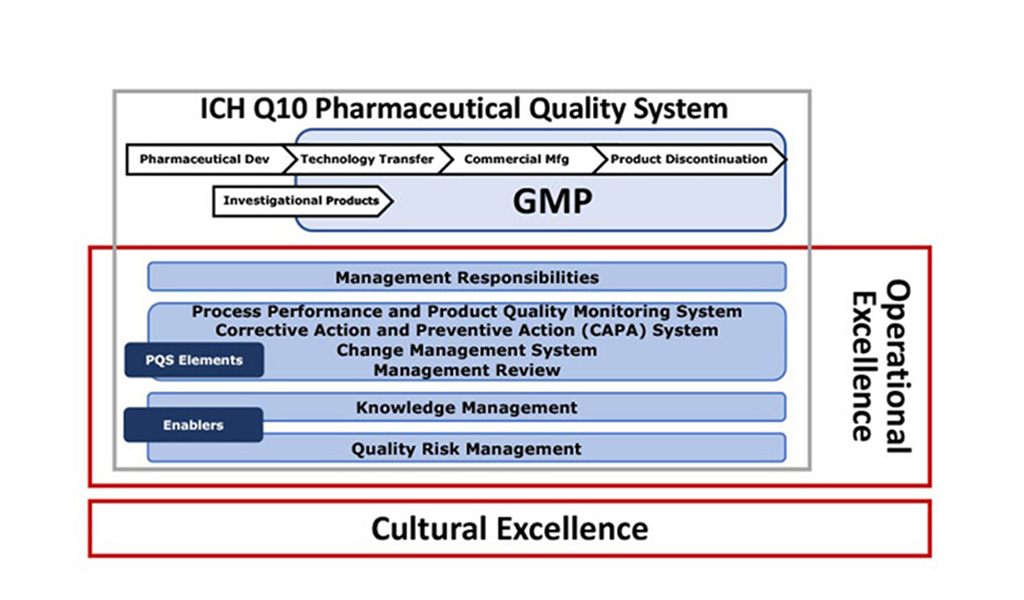
APQ 计划将包括基于四个 ICH Q10 制药质量体系 (PQS) 要素的五个指南;
- 纠正措施和预防措施 (CAPA) 系统
- 管理评审和管理职责
- 变更管理系统
- 过程性能和产品质量监控系统
- 下图显示了中心的四个指南,以及支持的知识体系。
纠正措施和预防措施 (CAPA) 以及管理评审和管理职责指南已经发布。变更管理指南计划于 2021 年底前发布,过程性能和产品质量监控指南将于 2022 年发布。
此外,最近出版了 ISPE 良好实践指南:制药行业的知识管理。
下图基于 ICH Q10 附件 2 PQS 模型显示了 APQ 计划及其指南如何补充 ICH Q10。